コンクリートの中性化とは
打設され硬化したコンクリートはpH12~13程度の強アルカリを示します。
これはコンクリートに水酸化カルシウムが多く存在しているためです。
コンクリート中にある鋼材(鉄筋)は周囲のコンクリートが強アルカリ性の間は、
不動態皮膜という酸化被膜に覆われて、腐食(水と酸素による化学反応)に対し抵抗し保護しています。
炭酸ガス(主に大気中の二酸化炭素)の作用を受けてコンクリート中の水酸化カルシウムが、
炭酸カルシウムに変化することにより、
コンクリートのアルカリ性がpH11以下になると、
鋼材を覆っている不動態皮膜が消失し、腐食しやすくなります。
大気中の二酸化炭素がどのようにコンクリート中の炭酸カルシウムに作用し、
どのように中性化が進展するのかについてのメカニズムを以下に説明します。
STEP-0
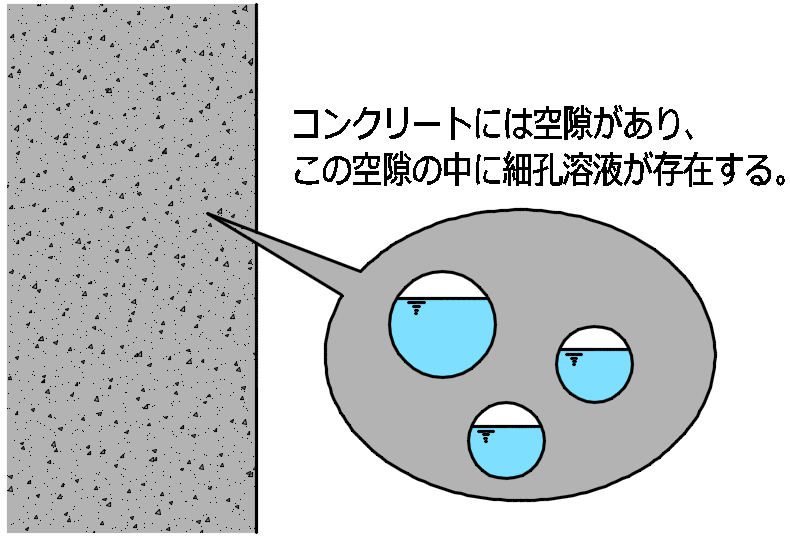
(0)コンクリートには空隙が存在しています。
コンクリートには空隙があり、この空隙の中に
細孔溶液(主に水和反応に使われなかった水分)が存在します。
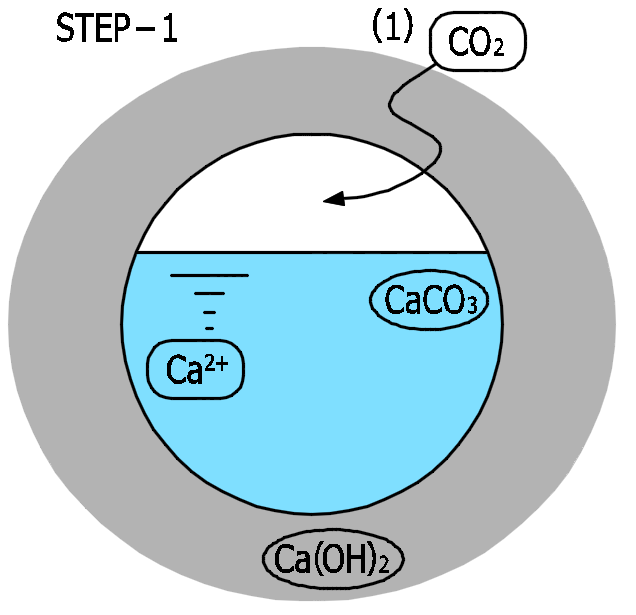
STEP-1
(1)コンクリートの空隙に二酸化炭素(\(CO_2\) )が入り込みます。
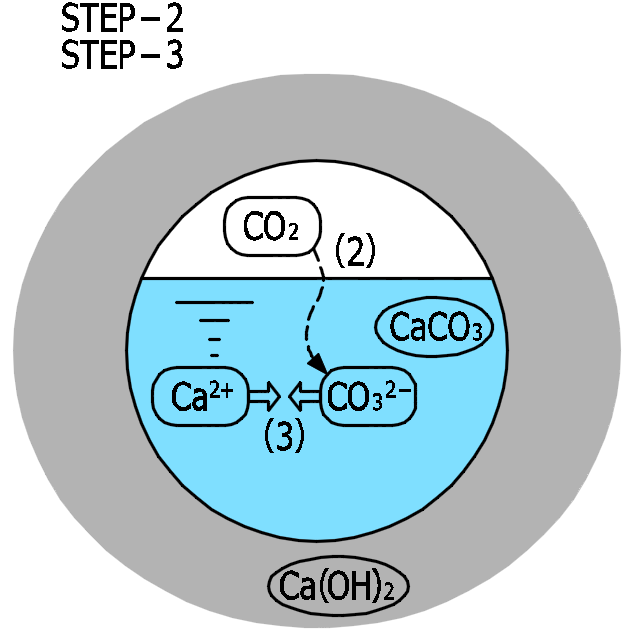
STEP-2
(2)空隙に浸入した二酸化炭素(\(CO_2\) )が細孔溶液に溶けて、
炭酸イオン(\(CO_3{ }^{2-}\) )となります。
=細孔溶液中の炭酸イオン濃度が高まります。
STEP-3
(3)炭酸イオン(\(CO_3{ }^{2-}\) )とカルシウムイオン(\(Ca^{2+}\))が反応し、
炭酸カルシウム(\(CaCO_3\) )が生成されます。
炭酸カルシウムは溶解度が低いため、細孔溶液に溶けずに沈積します。
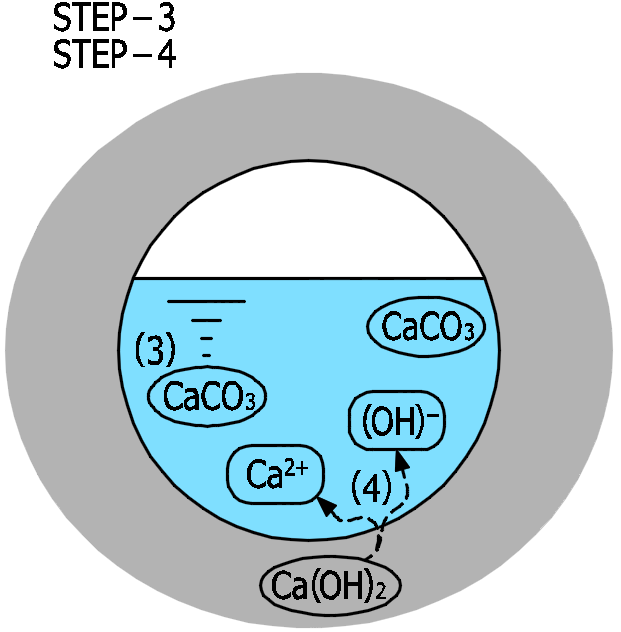
STEP-4
(4)STEP-3の反応で細孔溶液中のカルシウムイオンが消費されたことにより、
細孔溶液中のカルシウムイオン濃度が低くなります。
濃度平衡(細孔溶液中のイオン濃度を元濃度に戻そうとする働き)により
コンクリート固相に存在する水酸化カルシウム(\(Ca(OH)_2\) )が細孔溶液中に溶け出します。
STEP-5
(5)STEP-1~STEP-4の作用を何度も繰り返すことにより、
コンクリート中の水酸化カルシウムが消費され減少します。
つまり、コンクリートのアルカリ性が弱まります(=中性化が進展する)。
まとめ
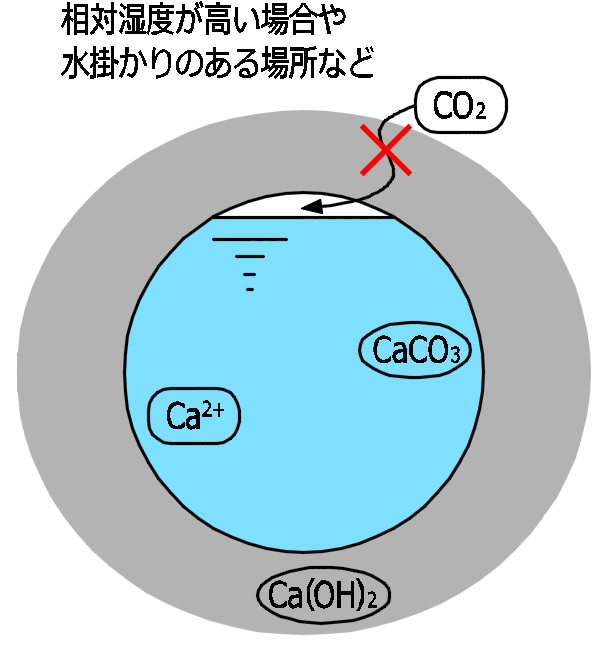
相対湿度が高い場合や、水掛かりがある場所の場合は、
空隙が水分で満たされ二酸化炭素の入り込む余地が小さくなるため、
上記のSTEP-1が生じにくくなるため、
中性化メカニズムのサイクルが起こらず
中性化の進展速度は遅くなります。
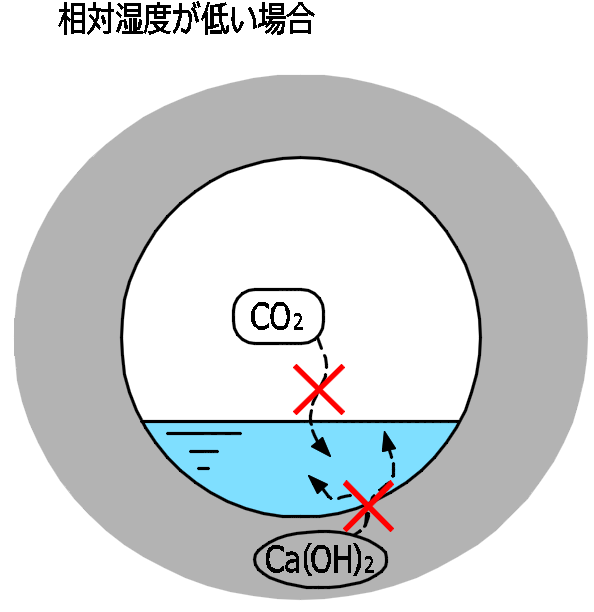
相対湿度が低い場合は、
コンクリートからの水分蒸発が多くなり、
細孔溶液の量が少なるなるため、
濃度平衡のサイクルが生じにくくなり、
この場合も、中性化の進展速度は遅くなります。
中程度の相対湿度(40~70%)のときに
コンクリートの中性化が進展しやすいのは、
これらのメカニズムによるためであると考えられています。

